da Leadership Medica n. 9 del 2003
Abstract
Dal momento che i sintomi di dell'embolia polmonare (EP) sono alcuni poco specifici, altri poco sensibili, per poter arrivare ad una diagnosi ad alta probabilità di EP vengono utilizzate diverse indagini: Rx torace, ECG, ECO, dosaggi D-Dimero, che ci aiutano più che a fare diagnosi di EP, vista la loro scarsa specificità, ad escludere od a porre diagnosi alternative o più probabili.
La diagnosi di EP è infatti è sia sottostimata che sovrastimata. E' sottostimata perché non sono diagnosticate in vita un terzo delle embolie massive e sub massive specie nei pazienti con malattie avanzate associate (cardiopatici, bronchitici cronici in particolare) o in caso di morte da improvvisa e tumultuosa insufficienza cardio-respiratoria.
E' anche sottostimata per l'imprecisione diagnostica ed il non riconoscimento dei diversi quadri clinici di presentazione, e nel non riconoscimento della loro gravità. L'imprecisione diagnostica (sottostima e sovrastima) dipende anche dalla scintigrafia polmonare perfusionale che è l'indagine più utilizzata per la diagnosi, ma che presenta una sensibilità non molto alta nella maggioranza dei casi (nel 60% circa non risulta diagnostica; in questo gruppo di pazienti solo i1 28% presenta un'EP all'angiografia polmonare.
La scintigrafia polmonare esclude la EP nel 15% dei casi (scan completamente negativo) e lo conferma nel 15% circa dei casi se risulta ad alta probabilità. Per questi motivi si è portati perciò a trattare quando non necessario per evitare eventi fatali. E' fiorita pertanto una grossa mole di lavori a livello internazionale con l'obiettivo di migliorare la strategia investigativa, evitando di sotto/sovrasimare la EP e di utilizzare il meno possibile le indagini radiologiche invasive.
Sono così stati introdotti nella diagnostica l'ecocolorDoppler (ECD) degli arti inferiori, la TC spirale polmonare, l'ecocardiografia, il dosaggio del D-Dimero. Il problema di conciliare le caratteristiche dei vari strumenti diagnostici con le esigenze cliniche è superabile solo con un approccio diagnostico probabilistico (probabilità percentuale di corretta diagnosi con accettazione dei falsi diagnostici) in assenza di strumenti che permettano un approccio deterministico con certezza di diagnosi.
Articolo
 L'embolia polmonare (EP) è una condizione patologica grave: se non tempestivamente riconosciuta e trattata risulta letale in circa il 10% dei casi.
L'embolia polmonare (EP) è una condizione patologica grave: se non tempestivamente riconosciuta e trattata risulta letale in circa il 10% dei casi.
I maggiori problemi sono quelli di tipo diagnostico poiché non esistono segni o sintomi patognomonici dell'EP e spesso non è agevole identificare, sulla sola scorta dei sintomi, la presenza di trombosi venosa profonda (TVP), che rappresenta la causa prima di EP in oltre l'80% dei casi (1).
L'EP rappresenta la terza causa di morte dopo lo stroke e l'infarto miocardico (6). Rappresenta l'1% delle cause di morte intraospedaliera, con un'incidenza stimata di un caso per mille nella popolazione generale non stratificata per età (2). L 'incidenza raddoppia ogni decade: è rara prima dei 40 anni (3), sicuramente più frequente sopra i 65 anni, interessa più frequentemente il sesso maschile che il femminile, ed è solo lievemente inferiore a quella dello stroke.
Secondo stime anglosassoni (4), confermate da recenti italiane, l' 1% della popolazione ospedaliera presenta una manifestazione di tromboembolismo venoso. L'incidenza della malattia tromboembolica negli Stati Uniti è stata stimata in circa 750.000 casi l'anno con 200.000-300.000 ricoveri ospedalieri (5), mentre in Italia si stima che ogni anno si verifichino 60.000 nuovi casi.
Un terzo degli episodi è fatale e la quasi totalità dei decessi avviene precocemente entro 1 ora dall'esordio dei sintomi. L'aumento dell'età media della popolazione ed il più elevato numero di pazienti che hanno una prolungata sopravvivenza in corso di malattie, neoplastiche, cardiache o polmonare, farà sì che nel futuro il problema possa divenire ancor più rilevante. È pertanto importante conoscere il corteo sintomatologico suggestivo di tale condizione.
Presentazione Clinica
L'EP è una condizione clinica potenzialmente fatale, caratterizzata da una presentazione clinica variabile e non vi sono segni o sintomi che possano essere considerati specifici per questa patologia. Ciononostante, la valutazione clinica del paziente con sospetta embolia polmonare, specie quando siano presenti eventuali fattori di rischio, deve essere accurata e critica, perché rimane il principale elemento guida nell'iter diagnostico.
La sintomatologia è estremamente variabile e riflette l'entità dell'impegno vascolare. Nelle forme non massive i sintomi più frequenti sono rappresentati dalla dispnea, dal dolore toracico, mentre la sincope è più frequente nelle forme massive (5).
Talora il paziente può lamentare anche dolore di tipo pleurico, causato da infarto polmonare o da embolia dei rami distali con conseguente irritazione pleurica. Una tachicardia inspiegata, l'improvvisa comparsa di tosse secca, specie notturna, possono essere gli unici elementi clinici che possono far orientare verso una microembolizzazione polmonare.
L'interessamento di vasi di maggior calibro si manifesta invece con la comparsa di dispnea grave ed improvvisa, mentre un dolore toracico similanginoso, da verosimile ischemia del ventricolo destro, è spesso espressione di una maggiore compromissione emodinamica.
Un episodio sincopale o una grave ipotensione fino allo shock sono infine espressione di una embolia polmonare massiva e si associano a segni e sintomi di ipoperfusione quali cianosi periferica e/o oliguria.
Diagnosi
L'EP è una sindrome di difficile diagnosi: è importante sospettare la malattia per poterla diagnosticare, ma dal momento che i segni ed i sintomi di EP non sono specifici (7 - 9), sono necessari dei test obbiettivi che ci consentano, in vivo, di confermarla od escluderla.
Elettrocardiogramma
Serve fondamentalmente per escludere altre diagnosi come la pericardite, l'IMA; può evidenziare un sovraccarico dx sistolico e/o diastolico (R alta in V1, BBdx di recente insorgenza) S1-Q3, T negative nelle precordiali (segno di ischemia da compressione delle coronarie con ischernia del ventricolo sx); risulta utile in particolare cioè nelle forme con disfunzione ventricolare dx.
Emogasanalisi
L'ipossiemia è un reperto molto frequente in corso di embolia polmonare, ma circa il 20% dei soggetti con EP (specie quelli giovani) presentano una normale pressione parziale di ossigeno.
Poiché l'ipocapnia è un reperto quasi costante all'emogasanalisi, è stato supposto che il riscontro di un'aumentata differenza alveolo-arteriosa di ossigeno potesse rappresentare un elemento diagnostico più sensibile di EP. I risultati di recenti studi sono stati però deludenti in questo senso, in quanto ben il 15-20% dei soggetti con EP presentano una normale differenza alveolo-arteriosa d'ossigeno (10).
Rx torace
Motivo dell'utilizzo: -esclusione di uno pneumotorace, polmonite, edema polmonare, cancro, altre patologie; -può essere suggestivo di EP quando c'è l'infarto polmonare od emorragia polmonare che può presentarsi come una opacità parenchimale od atelettasica semicircolare con la base che aggetta sulla superficie pleurica (51%) (20).
Nell'emorragia polmonare, l'opacità polmonare scompare entro una settimana, mentre nell'infarto dura anche 8-12 settimane.
Altre caratteristiche compatibili con EP sono il versamento pleurico (38%, con la caratteristica di essere piccolo, spesso interessante solo l'angolo costo-frenico), l'atelettasia subsegmentaria, l'infiltrato polmonare; raramente si osserva la oligoemia ( Westermark's sign. 11 %), l'oligoernia regionale con dallo stesso lato lo slargamento dell'arteria polmonare (Fleischer's sign).
E' pertanto utile nella presentazione clinica di infarto od emorragia polmonare, o in caso di collasso in soggetti con riserva cardio-polmonare ridotta per escludere altre malattie, diverse dall'EP, ma che la simulano (Figura 1).
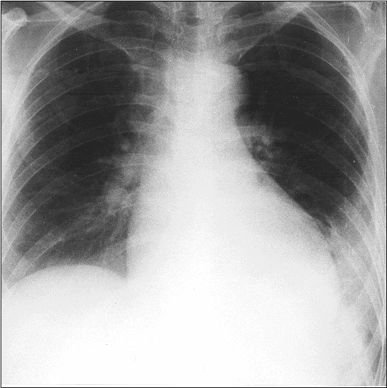 Figura 1: oligoemia al campo superiore dx (segno di Westermark)
Figura 1: oligoemia al campo superiore dx (segno di Westermark)
e opacità basale a sx (segno di Hampton)
Permette un'appropriata interpretazione della scintigrafia perfusionale polmonare perché in caso di normalità il difetto perfusorio eventuale allo scan acquista notevole probabilità di essere una EP, e l'interpretazione della scintigrafia è ottimale ed inoltre permette di identificare quelle alterazioni che causano un deficit perfusorio non embolico come; BPCO con grosse bolle di enfisema, bronchiectasie evidenti, fibrosi polmonare, interventi chirurgici, processi infettivi, importante cifoscoliosi, recente radioterapia (11).
Ecocardiogramma
L'ecocardiogramma è un esame non invasivo, disponibile in quasi tutti i centri che può risultare di notevole utilità nella diagnostica dell'embolia polmonare. Una dilatazione ed ipocinesia della parete libera del ventricolo destro, un aumentato rapporto RV/LV (causato dal bulging del setto nella cavità ventricolare sinistra), la dilatazione delle arterie polmonari prossimali, un aumentato rigurgito tricuspidalico (di solito a velocità intorno a 3-3,5 m/sec), ed infine una dilatazione della vena cava inferiore, insensibile alle escursioni respiratorie, sono elementi che orientano verso una diagnosi di embolia polmonare massiva (12). L'entità della compromissione funzionale del ventricolo destro risulta il fattore prognostico dotato di maggior potere predittivo di mortalità a breve termine.
Nessuno dei reperti ecocardiografici appare caratterizzato da elevata sensibilità e solo la diretta visualizzazione dell'embolo livello dell'arteria polmonare, con l'ecocardiografia transesofagea, consente di fare diagnosi di certezza di embolia polmonare.
Un ecocardiogramma normale comune esclude una embolia polmonare di rilevante impegno emodinamico anche se non consente di escludere con certezza condizioni caratterizzate da ripercussioni emodinamiche più limitate.
Per quanto riguarda tutte le situazioni intermedie (che costituiscono in realtà la maggior parte delle forme di embolia polmonare), il ruolo dell'ecocardiografia nella diagnostica dell'embolia polmonare merita di essere pienamente valutato, soprattutto nell'ambito di studi clinici prospettici, in particolare al fine di identificare pazienti con embolia polmonare che possano beneficiare di un trattamento trombolitico piuttosto che della terapia eparinica nonostante l'assenza di ipotensione sistemica o di shock (13).
Dosaggio d-dimero
Il D-Dimero (DD), è un prodotto di degrado della fibrina; esprime la attivazione della trombina e della fibrinolisi. Può essere misurato con metodi quantitativi (ELISA) o serniquantitativi (latex e simili, utilizzando monoclonali).
Mentre i test quantitativi in ELISA hanno bisogno di 5-6 ore per poter arrivare al risultato, i test semiquantitativi richiedono solo 20-30 minuti. Tutti i metodi per testare il DD sono stati validati in numerosi studi pubblicati e la loro accuratezza è stata stabilita. Il DD ha un valore predittivo negativo del 98% contro però una specificità del 35%, legata al fatto che la coagulazione può essere attivata da molte condizioni come il cancro, infezioni, malattie epatiche, scompenso cardiaco, interventi chirurgici, malattie infiammatorie.
Anche variando il cut-off si possono ottenere specificità maggiori ma sempre con una perdita in sensibilità non riuscendo a raggiungere un compromesso accettabile per un rapporto costo- beneficio favorevole.
Una review (14) che valuta l'utilizzo del DD da un punto di vista prettamente clinico per escludere la EP o TVP senza l'utilizzo di altri indagini, conclude che rimane ancora non provata la sua utilità.
Numerosi sono i motivi che rendono problematici il dosaggio del DD e la sua interpretazione clinica probabilistica nei pazienti che si presentano con sintomi (nei pazienti che si presentano asintomatici per TVP non è considerato utile dosare il DD (15) in quanto:
l) la presenza di altre malattie attivanti la coagulazione rendono il DD positivo,
2) dipende dal tempo di comparsa dei sintomi, perché anche se ci troviamo di fronte ad un paziente che non presenta patologia concomitante dopo 10 gg dall'evento trombizzante il DD risulta a1 95% negativo, pur in presenza di malattia,
3) per ultimo ma per questo non meno importante il rapporto costo - efficacia risente molto della prevalenza di malattia (16, 17), per cui sarebbe da utilizzare in caso di prevalenza di malattia bassa (18) da solo od in associazione con il Doppler venoso e con 1 'EGA (19).
 Figura 2: Angiografia polmone sx: Difetti di riempimento
Figura 2: Angiografia polmone sx: Difetti di riempimento
dei rami delle arterie del lobo inferiore sx (freccette)
Doppler venoso degli arti inferiori
EP e TVP degli arti inferiori possono essere considerate come parte di un'unica entità clinica definita “tromboembolismo venoso”.
Studi autoptici hanno infatti documentato che nel 90% dei soggetti con embolia polmonare è presente una trombosi a livello delle vene degli arti inferiori. Il rilievo strumentale di trombosi venosa profonda in pazienti con sospetta embolia polmonare è un elemento che induce a proseguire la terapia anticoagulante e rende sostanzialmente inutile un'ulteriore valutazione invasiva.
L'esame ultrasonografico in B-mode, integrato dalla metodica color Doppler si è dimostrato particolarmente utile specie nelle trombosi venose al di sopra del ginocchio.
La mancata comprimibilità del vaso venoso costituisce il criterio diagnostico dotato di maggior specificità, mentre minore valore diagnostico hanno il rilievo di una iperecogenicità intraluminale o di alterazioni del segnale color Doppler (20).
La diagnosi clinica di TVP, come ormai ampiamente sottolineato da numerosi studi, risulta scarsamente affidabile consentendo di formulare una diagnosi corretta in meno del 50% dei casi.
Anche se la maggior parte dei pazienti con embolia polmonare non ha sintomi o segni di trombosi venosa, la specificità dell'esame Doppler in pazienti con EP rimane alta (circa il 97%). Peraltro lo studio Doppler documenta una trombosi venosa solo nel 30-50% dei pazienti con provata embolia polmonare di modo che l'esame è dotato di elevata specificità ma scarsa sensibilità. Un normale esame Doppler non esclude pertanto la presenza di embolia polmonare.
Alcuni autori suggeriscono di effettuare uno studio Doppler delle vene degli arti inferiori qualora, pur in presenza di un sospetto clinico, l'esame scintigrafico sia risultato normale. Nell'eventualità che anche l'esame Doppler sia negativo, si pensa infatti che il rischio tromboembolico sia così basso da permettere la sospensione del trattamento anticoagulante. Si stanno valutando protocolli diagnostici che prevedano esami Doppler in serie in questi soggetti allo scopo appunto di migliorare la sensibilità del test (21).
La indagini non invasive di primo livello, in conclusione, possono risultare di aiuto nel confermare il sospetto diagnostico di embolia polmonare in attesa di una conferma definitiva della diagnosi.
T C spirale polmonare
La TC spirale è in grado di riconoscere gli emboli a livello dei tronchi polmonari ed a livello delle arterie segmentarie che vengono evidenziati come difetti di riempimento. Recenti affinamenti nella tecnica può portare la risoluzione anche a livello subsegmentario (22).
La percentuale degli emboli subsegmentari è stata stimata sul 6% e risultano pericolosi nei pazienti con riserva cardio-polmonare compromessa. La tecnica TC è sicuramente meno complessa della angiografia polmonare e sicuramente di più rapida esecuzione. La sensibilità e specificità per i trombi segmentali e centrali è alta (92%) (23 - 25), per cui è proponibile l'utilizzo:
1 Per pazienti con sospetto di EP con quadro di presentazione clinica severo (sincope, ipotensione, shock, o dispnea isolata improvvisa)
2 Va anche richiesta in presenza di anomalie all'Rx del torace, scintigrafia non diagnostica (Intermedia e bassa probabilità), ECD negativo in pazienti con riserva cardio- polmonare ridotta.
3 E' infine indicata nei pazienti con discrepanza tra probabilità scintigrafica e clinica, con ECD negativo in pazienti con riserva cardio-polmonare normale. In conclusione rimane difficile con le attuali evidenze considerare come gold standard la T C spirale polmonare; un suo sicuro vantaggio e' la possibilità di diagnosticare una malattia polmonare diversa dall'EP .
Gioca un ruolo diagnostico importante nelle forme a presentazione severa sia per conferma di EP che per diagnosi alternative (25, 26).
Scintigrafia polmonare
La scintigrafia polmonare ha un ruolo chiave nella diagnostica dell'embolia polmonare, essendo un esame non invasivo, ampiamente valutato in grandi trial clinici. Teoricamente la contemporanea acquisizione delle immagini perfusionali e ventilatorie consente di evidenziare eventuali difetti perfusionali in presenza di una normale fase ventilatoria, elementi che consentono una sicura diagnosi differenziale con condizioni nelle quali deficit di perfusione e di ventilazione possono coesistere.
Recenti dati dello studio PISAPED (27) hanno comunque evidenziato un elevato valore predittivo positivo e negativo della sola scintigrafia di perfusione qualora il sospetto clinico sia elevato.
Un importante limite dell'esame scintigrafico è rappresentato dall'ampia variabilità tra due osservatori che può raggiungere anche il 10-20%. Durante l'esame scintigrafico le immagini vengono acquisite almeno in sei proiezioni. Nella fase ventilatoria possono essere utilizzati vari traccianti, quali particelle di carbone marcate con tecnezio 99 oppure xenon 133.
Per la fase perfusionale vengono invece impiegate particelle di albumina marcata con Tecnezio 99, che, in presenza di una normale perfusione, si distribuisco in modo uniforme in tutto l'albero vascolare. In caso di ostruzione di un ramo arterioso, il distretto a valle apparirà “freddo”, privo cioè di marcante. Nello studio PIOPED (23) una scintigrafia considerata “ad elevata probabilità” si associa ad embolia polmonare nel 96% dei casi, tuttavia in pazienti con un esame definito “a bassa probabilità” è stata dimostrata l'esistenza di embolia polmonare anche nel 40% dei pazienti.
Nello studio PISAPED (27) è stata utilizzata esclusivamente la scintigrafia polmonare di perfusione e la diagnosi di embolia polmonare è stata formulata in presenza di difetti perfusionali a carico di uno o più segmenti al fine di cercare di eliminare esami a probabilità intermedia di malattia. Secondo questo schema di classificazione, un esame scintigrafico positivo è risultato avere un potere predittivo positivo del 95%, mentre un esame negativo un potere predittivo negativo del 81%.
Sulla base di questi studi, una scintigrafia polmonare normale esclude con almeno il 95% di probabilità una embolia polmonare così come un esame ad alta probabilità si associa alla presenza di embolia polmonare in quasi il 90% dei pazienti.
Rimane tuttavia un'ampia zona di ombra, costituita dagli esami di media e bassa probabilità, che globalmente costituiscono oltre il 70% dei casi. In questi pazienti la scintigrafia non offre alcun contributo diagnostico definitivo e solo la contemporanea valutazione clinica oltre che la ricerca di una possibile sede di origine dell'embolo possono indirizzare verso la diagnosi.
Se invece il dato scintigrafico è associato ad uno scarso sospetto clinico la probabilità che il paziente abbia una embolia polmonare sono inferiori al 5%. Di per sé invece i rilievi clinici, la radiografia del torace, l'ecocardiografia Doppler e le indagini di laboratorio possono essere di aiuto nel rinforzare il sospetto diagnostico, tuttavia hanno un limitato valore predittivo.
Studi prospettici hanno dimostrato che la presenza di una scintigrafia polmonare negativa identifica comunque una popolazione a basso rischio nella quale la terapia anticoagulante può essere sospesa. Quando la scintigrafia polmonare non sia conclusiva, un'embolia polmonare all'angiografia è stata dimostrata nel 25% dei casi. In questi pazienti quindi è necessario un approfondimento diagnostico prima di qualsiasi opzione terapeutica definitiva.
Angiografia polmonare
E' una tecnica invasiva che viene considerata come gold standard diagnosdco dell'EP (Figura 2). E' una tecnica non priva di rischi (0,5%) di mortalità (28), non è disponibile in tutti gli ospedali, presenta anche ad esperti radiologi difficoltà interpretative ed anche nelle forme subsegmentarie non è cosi precisa come in precedenza si credeva (29, 30).
E' utile nei casi a presentazione severa clinica in cui dopo la TC spirale bisogna con una certa rapidità fare diagnosi per attuare la terapia trombolitica; da evidenziare che le emorragie dopo angiografia sono sicuramente maggiori anche se non importanti quoad vitam. Può trovare un suo ruolo nei pazienti con riserva cardiopolmonare ridotta oltre che quando le indagini precedenti non hanno dato esito positivo.
Si sono costruiti e validati algoritmi diagnostici che tendono ad utilizzarla il meno possibile (31). Venografia arti inferiori Il razionale del suo utilizzo nella diagnostica di EP risiede nel fatto che l'origine dell'embolo ne1 70% dei casi è nelle vene degli arti inferiori.
Da ricordare che ne130% circa dei casi la sede di partenza non è negli arti inferiori. Il riscontro quindi di TVP autorizza quindi ad intraprendere l'anticoagulazione. Sebbene sia considerata il gold standard, la venografia ha un'accuratezza nell'evidenziare una TVP prossimale de160 % (31,32); inoltre non può essere utilizzata in caso di allergia al mezzo di contrasto, e nonostante la protezione del feto e la non estensione allo studio dei vasi pelvici non è da tutti accettata nella gravidanza.
Modelli Clinico-diagnostici
Nella pratica clinica è utile distinguere alcuni sottogruppi confermati da numerosi studi (33 - 36):
1.Frequenza: 4-5% dei casi Collasso circolatorio od ipotensione da sola od associata a perdita di coscienza; può essere presente dolore centrale toracico, o senso d'oppressione, debolezza, ortopnea, giugulari turgide.
L 'ECG spesso evidenzia le alterazioni considerate caratteristiche di EP; la radiografia del torace è spesso normale, i gas nel sangue evidenziano una ipocapnia associata ad importante ipossia che non si corregge con ossigenoterapia al 40%; l'esame fisico permette di evidenziare un soffio sistolico sulla tricuspide che si incrementa con l'inspirazione, un secondo tono rinforzato sulle polmonare con associato soffio sistolico, un battito parasternale.
Poichè molto spesso è presente una occlusione arteriosa polmonare estesa è utile eseguire una ecocardiografia che ci può confermare la diagnosi, evidenziando una disfunzione acuta ventricolare dx , o porre diagnosi alternative. L'ipertrofia del setto depone per disfunzione cronica. Vanno escluse: l'IMA ventricolare sinistro e destro, la polmonite fulminante. lo shock settico, il tamponamento cardiaco, la dissezione aortica, l'emorragia massiva, l'ipokaliemia grave.
2. Frequenza: 60% circa dei casi. Due o più dei seguenti sintomi: dolore toracico pleuritico, dispnea, peggioramento di dispnea, dolore toracico non retrostemale non pleuritico, emottisi, tachipnea, tachicardia. In questi pazienti la radiografia del torace può spesso presentare i segni considerati significativi di infarto ed emorragia polmonare, e localizzati nella sede del dolore pleuritico; l'ECO è il più delle volte normale; lo studio angiografico in questa vasta serie di pazienti evidenzia emboli periferici con occlusione lieve moderata del letto vascolare.
Così nella maggioranza dei casi l'emogasanalisi risulta normale, le alterazioni radiologiche regrediscono rapidamente (1-8 gg), spesso senza arrivare all'infarto polmonare. Le diagnosi alternative sono un folto groppo che va dall'infezione virale o batterica polmonare, alla polmonite, atelettasia postoperatoria, bronchite acuta, dolore muscolo scheletrico, pericardite, pleurite, spasmo esofageo. n dolore dell'EP non cambia mai con gli atti del respiro; molto difficile è la diagnosi differenziale nei soggetti con malattia ostruttiva cronica polmonare. E' sicuramente il groppo di pazienti più cospicuo e con le maggiori difficoltà diagnostiche.
3. Frequenza: 25% circa dei casi Dispnea isolata ad esordio improvviso Il trombo di solito è centrale e questo si riflette sull'emogasanalisi che risulta sempre alterata, la tachipnea molto frequente, possono essere presenti dei segni di ipertensione polmonare acuta, la pressione è sempre normale nei soggetti con riserva cardiorespiratoria normale, non ci sono anomalie all'ECG, l'Rx del torace il più delle volte è negativo è utile eseguire un'ecocardiografia per escludere una disfunzione ventricolare dx che peggiora la prognosi. Quindi, una dispnea acuta in soggetto con fattori di rischio deve far pensare ad un 'EP.
4.Nel rimanente 10% dei casi Vanno considerati quei pazienti, di solito anziani, che presentano un'opacità polmonare alla radiografia, spesso accompagnata da dispnea e/o TVP pregressa. Un piccolissimo gruppo è dato da pazienti con scarsa riserva funzionale: vanno definiti tali i pazienti che presentano una malattia cronica polmonare: o cardiaca sintomatica che vanno incontro a scompenso della patologia preesistente per la comparsa di un'embolia polmonare periferica.
In questi casi l'ECG, l'Rx del torace e l'emogasanalisi non sono utili perché riflettono la sottostante malattia: spesso l'embolia è ricorrente con alta mortalità per non riconoscimento della EP, l'interpretazione della scintigrafia polmonare: è molto difficile.
Sarebbe necessaria l'angiografia polmonare.
La TC polmonare è scarsamente diagnostica. E' un gruppo numericamente esiguo, che pone però seri problemi nella diagnosi.
Dottor Francesco Imperatore
Servizio di Anestesia e Rianimazione, Dipartimento di Emergenza e Accettazione Azienda Ospedaliera
di Rilievo Nazionale “A. Cardarelli”, Napoli
Bibliografia
1. Stein PD, Henry JW: Prevalence of acute pulmonary embolism among patients in a general hospital and at autopsy. Chest 1995; 1.08:978-81.
2. Anderson Fa Jr, Wheeler HB , Go1dberg RJ, et all. A population based perspective of the hospital incidence of deepvein thrombosis and pulmonary embolism: The Worchester DVT Study. Arch. Intern Med 1991; 151:933- l. 3.Kniffin WD, Baron JA, et all. The epidemiology of diagnosed pulmonary embolism and deep vein thrombosis in the elderly. Arch Intern Med 1994; 154:861-6.
4. Samuel Z, Goldhaber. Pulmonary Embolism. N Eng J Med 1998; 339:93-104
5. ACCP Consensus Committee on Pulmonary Embolism. Opinions regarding the diagnosis and management of venous tbromboembotic disease. Chest 1.996; 1.09:233-7
6. Corris P, Ellis D, Foley N, Miller A. British Thoracic Society, Standards of care Commettee. Suspected acute pulmonary embolism: a practical approach. Thorax 1.997; supplement 4: s8-sl.l
7. Wells P, Jeffrey S, Ginsberg MD, et all. Use of a clinical model for safe management of patient with suspected pulmonary embolism. Ann Inter Med 1998; 129:997-1005
8. Hildner Fj, Ormond RS. Accuracy of the clinical diagnosis of pulmonary embolism. JAMA. 1967; 202:567-70
9. Sasahara AA, Sharma GV, Barsamian EM, et al. Pulmonary Embolism. diagnosis and treatment JAMA. 1983; 249:2945-50
10. Goldhaber SZ, De Rosa M, Visani I. ICOPER. Circulation 1.997; 96: Suppl.
11.Kasper W ,Kostantinides S, Geibel A, et Al. Management strategies and determinants of outcome in acute major pulmonary embolism: result of a multicenter registry. J Am Coll Cardio1997; 30:1165-71.
12. Edwin JR. Monique C, Tiel V B, et all. The value of lang scintigraphy in the diagnosis of pulmonary embolism. NEJM 1993; 20:173-181
13. Goldhaber SZ, Visani L, DeROSA M. Acute pulmonary embolism: clinical outcomes in the International Cooperative Pulmonary Embolism Registry. Lancet 1999; 353:1386-9
14. Becker D, Philbrich J , Bachhuber T, et all. D-dimer testing and acute venous thromboembolism. Arch Intern Med 1997; 156:939-46
15. Crippa L, D' Angelo V.S., Tomassini L, et all. The Utility and cost-effectiveness of D-dimer measurements in the diagnosis of deep vein thrombosis. Haematologica 1997; 446-52
16. Boanemaux H. de Moorleose P, Perrier A, et all Thromb Haemost 1994; 71: 1-6
17. Arnaud Perrier. Non invasive diagnosis of pulmonary embolism. Haematologica; 1997; 82: 328-31
18. Yague S, A normal D-dimer test is useful in excluding pulmonary embolism. JAMA 1993; 270:2819-22
19. Egermayer P, Town GI, Tumer JC, et all. Usefulness of D-dimer, blood gus, respiratory rate measurement for escluding pulmonary embolism. Torax 1998; 53:830-4 53
20. Modan B, Sharon E, Jelin N. Factors contributing to the incorrent diagnosis of pulmonary embolic disease. Chest 1972; 62: 388-93
21. AHA Consultation with the Council on Cardiovascolar Radiology, American Heart Association. Hirsh J, Hoak J. Management of Deep vein thrombosis and pulmonary embolism. 1998. Stein PD, et all. PIOPED J N M, t996; 37:577-81 22.Teigen C L, Maus T P, Sheedy P F, et all. Pulmonary embolism: diagnosis with contrast enhanced electro beam CT and comparison with angiography. Radiology 1995; t94: 3 t3-9
23. Stein PD, et all. PIOPED J N M, t996; 37:577-81
24. Remy G, Remy J, Artaud d, et all. Peripheral pulmonary arteries: optimization of the spiral tc protocol. Radiology 1997; 204:157-63
25. Holbert JM, Costellol P, Federle MP .Role of spiral tc in the diagnosis of pulmonary embolism in the emergency department Ann Emerg Med 1999; 33: 520-8
26. Kim KI, Muller NL, Majo JR Clinically suspected pulmonary embolism : utility of spiral CT .Radiology 199; 210: 693-7
27. Miniati M, Pistolesi M, Marini C. et all. Value of perfusion sacn in the diagnosis of pulmonary embolism: PISA- PED. Am J Respir Crit Care Med.1996; 154: 1387-93
28. Jarden R, Remj J, Wattime L, et all Central pulmonary thromboembolism : diagnosis with the single breath hold comparison with pulmonary angiography. Radiology t 992; 185 :38 t –7
29. Stein PD, Hull RD, Relative risks of anticoagulation treatment of acute pulmonary embolism based on an angiographic diagnosis versus V/Q scan. Chest 1994; 106:727-730
30. Pulmonary Embolism .Williams A. NucMed .1988
31. Stein PD, Athanasoulis C, Alavi A, et al. Complication and validity of pulmonary angiography in acute pulmonary embolism.Circulation. 1992; 85: 462-8
32. Alastair J.J., Wood. Management of Venous Thromboembolism. N Eng J Med 1996; 335:24, 1817-1828
33. Barrit DW, Jordan SC,. Clinical features of pulmonary embolism. Lancet 1961; 729-33
34. Stein PD, Willis PW, Demets. History and physical examination in acute pulmonary embolism in patients without preexisting cardiac or pulmonary disease. Am J CardioI. 1981;47:218-23
35. Stein PD, Terrin ML, Hales CA, et al. Clinical, Laboratory, roengten elettrocardiografic findings. Chest 1991; 100: 598-603
36. Palla A, Petrozzelli S, Donnamaria V, Giuntini. The role of suspicion in the diagnosis of pulmonary embolism. Chest 1995; 107:S 21-4




